大多数人会将神经系统疾病与脑部疾病划上等号——然而,神经系统疾病的复杂性远不止如此!
Category: Recent Development
癌症患者福音:高剂量率近距离放疗
癌症的高发病率和高死亡率让很多人谈癌色变。世卫组织数据显示,癌症是威胁人类健康的主要因素之一,2020年,有近1000万人死于癌症。
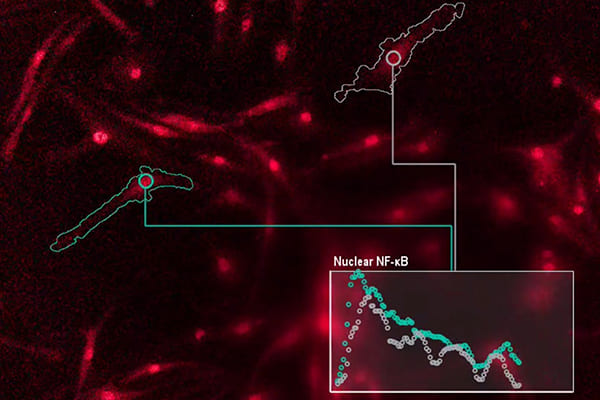
科学家破解免疫细胞的“语言”
免疫系统是保护人体免受感染的复杂细胞和蛋白质网络。免疫系统内保存了它曾经清除过的每一种微生物的记录,因此,当这些微生物再次进入人体时,免疫系统就可以迅速识别并速消灭它们。
通过饮食提升免疫力
新冠肺炎疫情在全国引发焦虑和恐慌,促使许多人迫切探索保护自己身体健康的最佳方法。虽然没有什么灵丹妙药可以预防生病,但适当的营养是帮助您保持健康和强壮的方法之一。
无论婴儿们正在学习几门语言,他们都更喜欢说”儿童语言”
有没有发现,当你和可爱的婴儿说话时,你很难不控制自己不去使用夸张的唱歌语调,这些其实都是有充分理由的。UCLA加州大学洛杉矶分校语言习得实验室和全球其他16个实验室的一项共同研究表明,无论婴儿们习惯听哪种语言,他们都会更爱说更关注儿童语言”。
UCLA Health医疗中心收到2900万美元的捐赠,用于建立精确基因组医学中心
UCLA Health医疗中心收到了2900万美元的捐赠,用于建立一个科学家和医生能够并肩工作的中心,研究基因在疾病中的作用,并开发改善遗传病患者生活的治疗方法。
悲伤造成的痛苦并不仅体现在心理层面
悲痛、心痛、忧虑、心碎——每一个词都在悲伤的情绪和它对人体的深远影响之间划出了一条直线。悲伤的人说他们感到空虚和麻木,因为悲伤而生病。
第二剂新型冠状病毒疫苗会带来什么
随着新冠疫苗在全国推广,人们对潜在副作用的好奇和担忧越来越多,尤其是对两针方案中的第二针。
UCLA Health医疗中心开创性的基因疗法让塞尔维亚女孩拥有健康生活的机会
在欧洲部分地区,Sofija Markuljevic被称为“统一了塞尔维亚的小女孩”。
成千上万的支持者通过杂志、电视和社交媒体关注着这个20个月大的孩子的旅程,从她被诊断出患有神经遗传性疾病,到她父母的筹款活动,再到她横贯大陆前往UCLA Health医疗中心接受拯救生命的治疗。
正念冥想对乳腺癌康复患者的好处
正念或关注当下对你的健康有益,这已经不是什么秘密了。但研究人员仍在发掘正念冥想的全部潜力,以及它如何有益于癌症患者。